빅테그라비르/엠트리시타빈/테노포비르 알라페나미드
| 복합약 | |
|---|---|
| 빅테그라비르 | 통합효소 억제제 |
| 엠트리시타빈 | 역전사효소 억제제 |
| 테노포비르 알라페나미드 | 역전사효소 억제제 |
| 식별 정보 | |
| CAS 등록번호 | 2097023-87-3 |
| ATC 코드 | J05AR20 |
| PubChem | ? |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B3(오스트레일리아)[1]?(미국)[1] |
| 법적 상태 | |
| 투여 방법 | 월별 |
빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)는 상품명 빅타르비(Biktarvy)로 판매되고 있는, HIV/AIDS치료를 위한 고정 용량 복합제 항레트로 바이러스 약물이다. 이 약물은 50mg의 빅테그라비르(Bictegravir), 200mg의 엠트리시타빈(emtricitabine), 25mg의 테노포비르(tenofovir)가 함유되어 있다.[3]
미국에서 2018년 2월에 사용승인되었고,[4][5] 유럽연합(EU)에서는 2018년 6월 사용승인받았다.[6]
병용 요법[편집]
빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)는 인간 면역 결핍 바이러스 치료를 위한 완전한 요법으로 사용할 수 있는 복합 약물의 예이다.[3]
종종 고 활성 항레트로 요법(HAART)라고 불리는 HIV 병용 요법은 두 유형 이상의 항 레트로 바이러스 약물로 구성된다. 병용 요법은 HIV-1균주가 병용에 사용되는 모든 약물에 내성을 획득 할 만큼 충분한 돌연변이가 될 가능성이 없기 때문에, 약물 내성이 발생할 가능성을 줄여준다. 병용 요법은 HIV-1환자의 수명을 늘리고 바이러스 전파 가능성을 크게 줄일 수 있다.[7]
구성[편집]

빅테그라비르(Bictegravir)(BIC)는 인테그레이즈 가닥 전달 억제제(INSTI)이다. 빅테그라비르(Bictegravir)는 다리로 연결된 bicyclic ring과 2,4,6-trifluorobenzyl group이 있는 별개의 벤질(benzyl) 꼬리를 포함하고 있기 때문에 다른 INSTI와는 다르다. 이것은 혈장 단백질 결합의 증가와 Pregnane X수용체(PXR)의 활성화 감소에 기여한다. 이러한 변화는 약물 간의 상호작용르 최소화 하고 청소율을 낮추며 용해도를 높인다. 빅테그라비르(Bictegravir)는 같은 등급의 다른 약물에 비해 약물 내성이 낮은 것으로 밝혀졌다.[8]
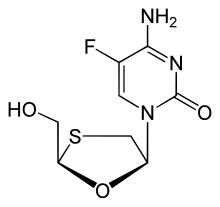
엠트리시타빈(emtricitabine)(FTC)은 티아시티딘(thiacytidine)의 합성 플로오르 유도체로 뉴클레오시드 역전사 효소 억제제(NNRI)이다. 세포 내에서 엠트리시타빈(emtricitabine)은 인산화되어 세포 내에서 에미티리시타빈 5'-삼인산(emitricitabine 5'-triphosphate)을 형성한다. 이것은 약물이 바이러스 및 숙주 기질과 경쟁하게 하고 궁극적으로 DNA사슬 연장의 종결을 야기한다.[9] 기저 B형 간염 바이러스(HBV)는 엠트리시타빈(emtricitabine)과 상호작용하여 심각한 간 손상을 일으킬 수 있지만 HBV가 없는 환자에게 투여 했을 때 간에 심각한 부작용은 없다.[10]

테노포비르 알라페나미드(tenofovir alafenamide)(TAF)는 뉴클레오타이드 역전사 효소 억제제(NRTI)로 기능하는 테노포비르(tenofovir)의 전구약물이다. 테노포비르(tenofovir)에 대한 다른 전구 약물이 테스트되었지만, TAF는 HIV-1치료를 개선하는데 더 효과적이다. 이 약물은 세포 내에서 HIV표적 세포의 대사 산물인 TFV 다이포스페이트(diphosphate)로 전환된다.[11] 따라서 TAF는 다른 테노포비르(tenofovir) 전구약물 보다 활성 대사산물의 농도는 더 높고, 혈장 TFV의 농도는 낮다.[12] TAF는 주로 신장에 의해 대사 되며 다른 전구약물보다 복용량이 적기 때문에 신장 배설계에 덜 해롭다.[11]
의료용으로 사용[편집]
이 약물 요법은 이전에 항 레트로 바이러스 치료를 받지 않은 HIV-1감염 성인 또는 ml당 50개 미만의 HIV-1 RNA copies을 가진 성인을 대상으로 한다. HIV-1환자는 이전에 빅테그라비르(Bictegravir), 엠트리시타빈(emtricitabine) 또는 테노포비르 알라페나미드(tenofovir alafenamide)에 대한 부작용이나 내성이 없어야 한다.
부작용[편집]
이 약물은 도페틸리드(dofetilide) 또는 리팜핀(rifampin)과 함께 투여해서는 안된다. 빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)와 함께 복용 할 때 도페틸리드(dofetilide)는 도페틸리드(dofetilide) 혈장 농도를 증가시켜 사망으로 이어질 수 있다. 리팜핀(rifampin)과 빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)를 함께 복용하면 빅테그라비르(Bictegravir) 혈장 농도가 감소하고 빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)에 대한 내성이 발생할 수 있다. 다른 HIV-1항 레트로 바이러스 약물은 이 요법과 함께 복용해서는 안된다.
신장 질환이나 신장 장애가 나타나면 약물을 중단해야 한다. B형간염 및 HIV-1환자에서 빅테그라비르(Bictegravir)/엠트리시타빈(emtricitabine)/테노포비르 알라페나미드(tenofovir alafenamide)의 중단은 B형 간염의 유병률을 증가시켜 간 대상부전과 간부전을 유발하는 것으로 나타났다.
약물 유해반응에는 설사, 메스꺼움, 두통이 포함되나 이에 국한되지는 않는다.[3]
각주[편집]
- ↑ 가 나 “Bictegravir / emtricitabine / tenofovir alafenamide (Biktarvy) Use During Pregnancy”. 《Drugs.com》. 2019년 9월 16일. 2020년 3월 7일에 확인함.
- ↑ “Biktarvy 50 mg/200 mg/25 mg film-coated tablets - Summary of Product Characteristics (SmPC)”. 《(emc)》. 2020년 8월 25일. 2020년 8월 26일에 확인함.
- ↑ 가 나 다 라 “Biktarvy- bictegravir sodium, emtricitabine, and tenofovir alafenamide fumarate tablet”. 《DailyMed》. 2019년 8월 8일. 2020년 3월 7일에 확인함.
- ↑ “Drug Approval Package: Biktarvy (bictegravir, emtricitabine, and tenofovir alafenamide) Tablets”. 《U.S. Food and Drug Administration (FDA)》. 2018년 3월 19일. 2020년 3월 7일에 확인함.
- ↑ “U.S. Food and Drug Administration Approves Gilead's Biktarvy (Bictegravir, Emtricitabine, Tenofovir Alafenamide) for Treatment of HIV-1 Infection” (보도 자료). Gilead. 2018년 2월 7일.
- ↑ “Biktarvy EPAR”. 《European Medicines Agency (EMA)》. 2020년 1월 21일. 2020년 3월 7일에 확인함.
- ↑ “FDA-Approved HIV Medicines Understanding HIV/AIDS”. 《AIDSinfo》 (미국 영어). 2021년 1월 27일에 원본 문서에서 보존된 문서. 2018년 5월 22일에 확인함.
- ↑ Tsiang M, Jones GS, Goldsmith J, Mulato A, Hansen D, Kan E, 외. (December 2016). “Antiviral Activity of Bictegravir (GS-9883), a Novel Potent HIV-1 Integrase Strand Transfer Inhibitor with an Improved Resistance Profile”. 《Antimicrobial Agents and Chemotherapy》 60 (12): 7086–7097. doi:10.1128/AAC.01474-16. PMC 5118987. PMID 27645238.
- ↑ “Emtricitabine”. 《Pubchem》. U.S. National Library of Medicine. 2018년 5월 22일에 확인함.
- ↑ “Emtricitabine Dosage, Side Effects”. 《AIDSinfo》 (미국 영어). 2020년 9월 1일에 원본 문서에서 보존된 문서. 2018년 5월 22일에 확인함.
- ↑ 가 나 Ray AS, Fordyce MW, Hitchcock MJ (January 2016). “Tenofovir alafenamide: A novel prodrug of tenofovir for the treatment of Human Immunodeficiency Virus”. 《Antiviral Research》 125: 63–70. doi:10.1016/j.antiviral.2015.11.009. PMID 26640223.
- ↑ “Tenofovir Alafenamide Information for Providers”. 《AIDSinfo》 (미국 영어). 2020년 9월 2일에 원본 문서에서 보존된 문서. 2018년 5월 22일에 확인함.
외부 링크[편집]
- “Bictegravir”. 《Drug Information Portal》. U.S. National Library of Medicine.
- “Emtricitabine”. 《Drug Information Portal》. U.S. National Library of Medicine.
- “Tenofovir alafenamide”. 《Drug Information Portal》. U.S. National Library of Medicine.
